
北京海岸鴻蒙標(biāo)準(zhǔn)物質(zhì)技術(shù)有限責(zé)任公司
 白金會員
白金會員 已認(rèn)證
已認(rèn)證

北京海岸鴻蒙標(biāo)準(zhǔn)物質(zhì)技術(shù)有限責(zé)任公司
 白金會員
白金會員 已認(rèn)證
已認(rèn)證
《藥品抽檢探索性研究原則及程序》要點解讀
一,、化學(xué)藥
問:藥品探索性研究要點中化學(xué)藥應(yīng)該重點關(guān)注,?
答:
口服固體制劑:針對標(biāo)準(zhǔn)較簡單、關(guān)鍵質(zhì)量控制指標(biāo)缺失或存在一定問題,、未通過一致性評價的仿制藥,、地標(biāo)升國標(biāo)等品種,建議重點關(guān)注溶出度,、釋放度,、有關(guān)物質(zhì)、元素雜質(zhì)殘留,、有機(jī)溶劑殘留等研究,。
已經(jīng)通過一致性評價的品種,除承檢機(jī)構(gòu)發(fā)現(xiàn)可能影響藥品質(zhì)量的問題外,,不建議做大量的溶出度探索性研究,,可通過適當(dāng)?shù)呐g溶出曲線比較,考察其工藝穩(wěn)定性和一致性情況,。
注射劑:重點關(guān)注與臨床給藥方式相關(guān)的用藥合理性,、安全性、有關(guān)物質(zhì),、滲透壓,、添加劑(穩(wěn)定劑,、抗氧劑、助溶劑,、等滲劑等),、pH值、溶液澄清度與顏色,、不溶性微粒與可見異物等方面,。
無菌分裝的注射用粉針:重點關(guān)注晶型、溶液的澄清度與顏色,、有關(guān)物質(zhì),、溶劑殘留、包材(如膠塞)相容性,、包材(如硅硼玻璃)多種元素雜質(zhì)的殘留,;對于有可能產(chǎn)生聚合物的品種,建議考察其聚合物的水平,,并應(yīng)評價測定方法的科學(xué)性和合理性,,考察聚合物與有關(guān)物質(zhì)之間的相關(guān)性;探討有關(guān)物質(zhì)測定方法取代聚合物測定方法的可行性,;考察不同方法測定結(jié)果之間的相關(guān)性,。
滴眼劑:該劑型屬無菌制劑,應(yīng)對其安全性給予關(guān)注,,參考注射劑項下相關(guān)要求進(jìn)行研究,,同時應(yīng)重點關(guān)注滲透壓、pH,、無菌,、可見異物、不溶性微粒,、金屬性異物等研究項目,;關(guān)注緩沖劑與抑菌劑種類、用量合理性,、抑菌效力及其對藥物穩(wěn)定性的影響,;關(guān)注開啟后的微生物污染情況;適當(dāng)考慮對滴眼液的黏度的評價,,分析處方的合理性,、工藝穩(wěn)定性和使用中的穩(wěn)定性;適當(dāng)考慮包裝材料,、容器或包裝方式對其抑菌效力等質(zhì)量穩(wěn)定性的影響,。
二、生化藥品
問:生化藥品中的動物來源生化藥品要關(guān)注什么呢,?
答:關(guān)注動物的種屬是否存在混用或代用,;通過考察組胺,、動物感染微生物的蛋白或核酸殘留來驗證使用的動物是否符合檢疫的要求;關(guān)注生產(chǎn)工藝能否有效去除雜蛋白或核酸殘留,;關(guān)注添加劑與滲透壓,;關(guān)注高分子物質(zhì);考察輔料對含量測定的干擾,;關(guān)注活力測定方法的專屬性;關(guān)注抗生素殘留問題,;關(guān)注標(biāo)準(zhǔn)中未涉及的安全性項目(如:過敏反應(yīng),,異常毒性,熱原或細(xì)菌內(nèi)毒素等),。
三,、中成藥
問:中成藥需要關(guān)注的項目都有?
答:口服制劑-藥材,、飲片,;生產(chǎn)工藝;質(zhì)量控制,;安全性,。注射劑-生產(chǎn)工藝、外觀,、添加劑,、滲透壓、高分子雜質(zhì),、質(zhì)量控制,。軟膏劑-生產(chǎn)工藝、添加劑,、質(zhì)量控制等,;關(guān)注微生物限度或無菌、防腐劑用量合理性及抑菌效力,、含細(xì)粉軟膏劑的粒度,。
四、生物制品
問:生物制品關(guān)注哪些,?
答:生產(chǎn)工藝,;不同企業(yè)產(chǎn)品質(zhì)量的相似性;質(zhì)量標(biāo)準(zhǔn)制定的科學(xué)性和合理性中關(guān)注可見異物,、微細(xì)可見異物及不溶性微粒等的分布及來源,;包材相容性關(guān)注包材中元素的遷移情況,包括重金屬離子,、抗氧劑(農(nóng)殘),、有機(jī)物等,;其他質(zhì)量擴(kuò)展研究。
《藥品抽檢探索性研究原則及程序》配套標(biāo)準(zhǔn)物質(zhì)解決方案
一,、
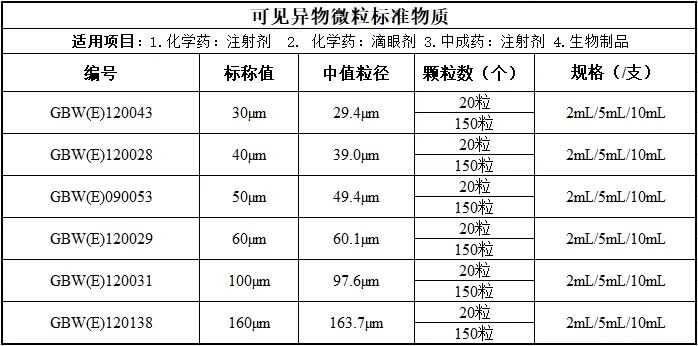

二,、

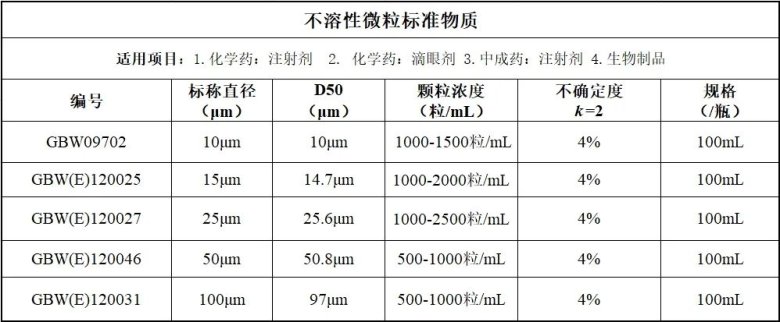


三、
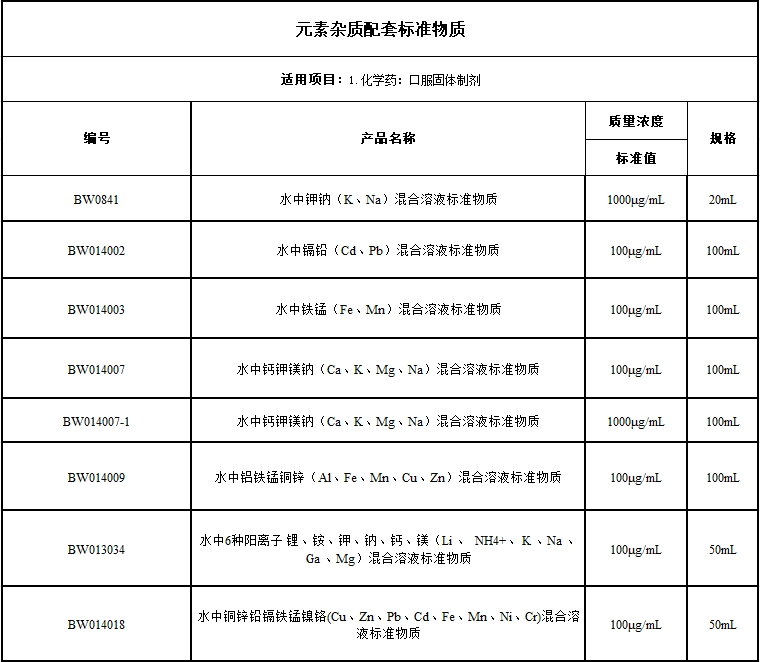
四,、
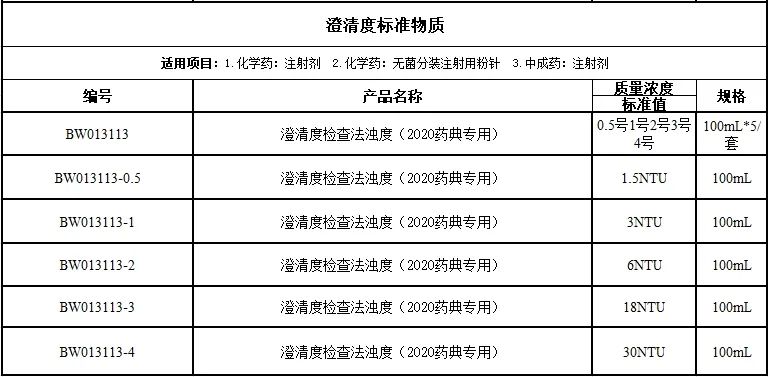
五,、
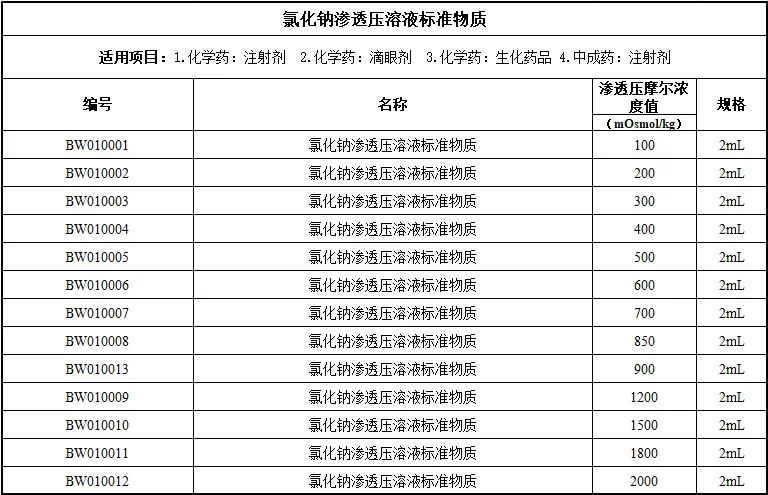
六、
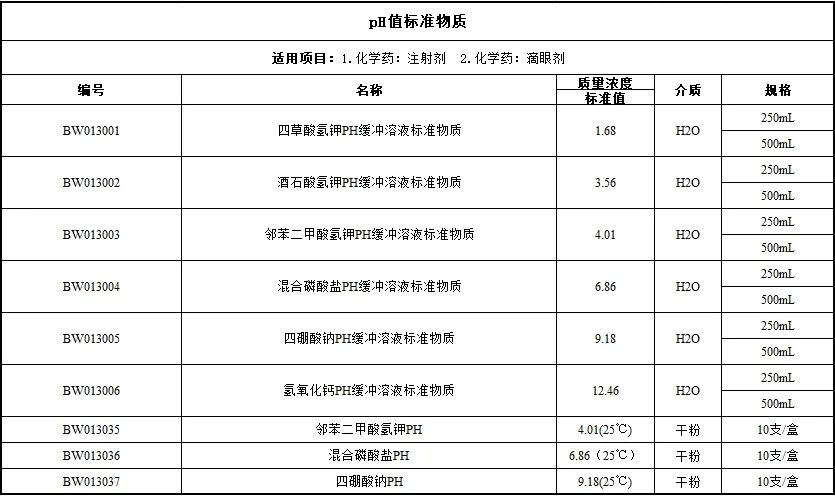

七,、
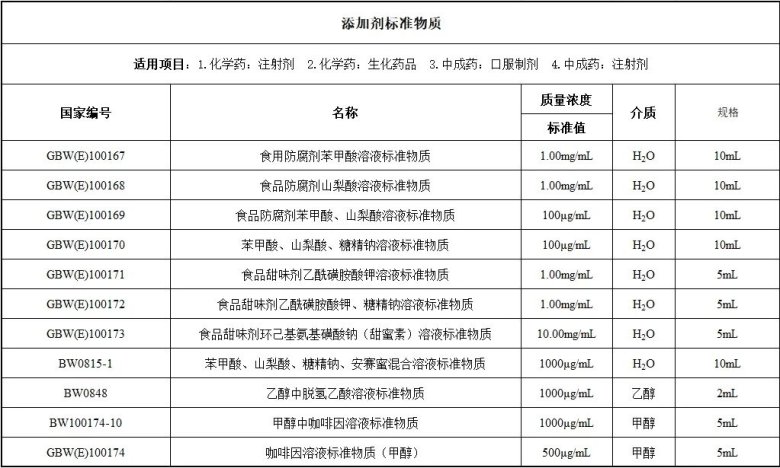
八,、
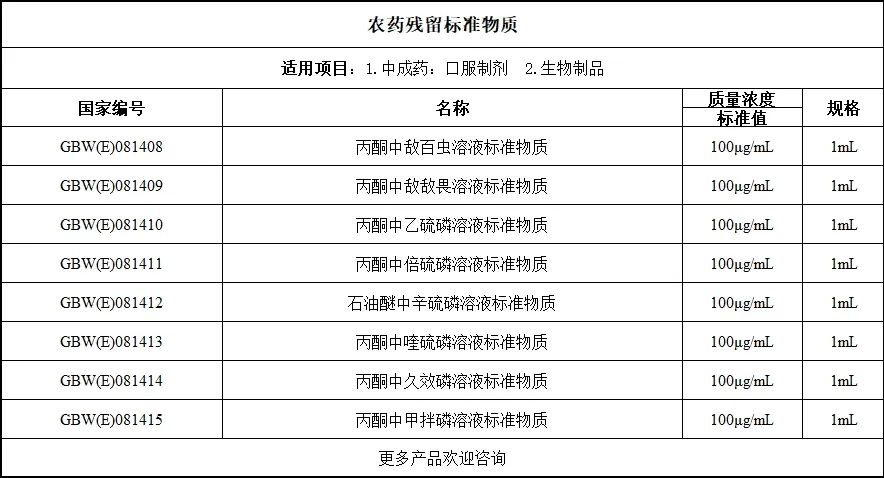

九、
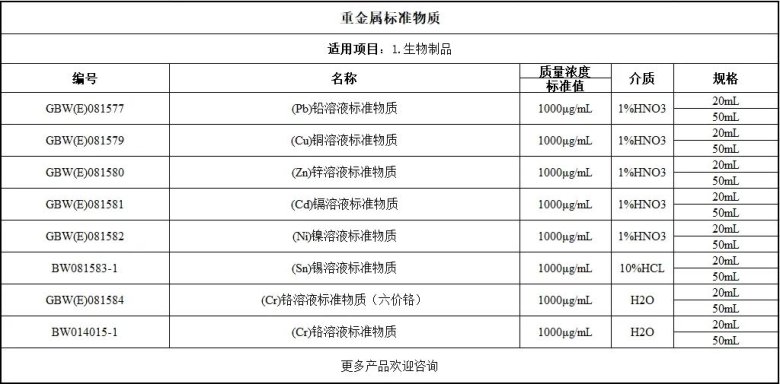
最新動態(tài)
更多



虛擬號將在 秒后失效
使用微信掃碼撥號