
北京海岸鴻蒙標(biāo)準(zhǔn)物質(zhì)技術(shù)有限責(zé)任公司
 白金會(huì)員
白金會(huì)員 已認(rèn)證
已認(rèn)證

北京海岸鴻蒙標(biāo)準(zhǔn)物質(zhì)技術(shù)有限責(zé)任公司
 白金會(huì)員
白金會(huì)員 已認(rèn)證
已認(rèn)證
12 月 21日,,輝瑞旗下無菌注射劑部門 Hospira 宣布了兩次獨(dú)立的召回,,原因是某些藥物的小瓶和注射器中可能存在玻璃顆粒。Hsopira一年發(fā)生過多次召回事件,,卻并沒有更進(jìn)一步解決玻璃顆粒污染問題,。
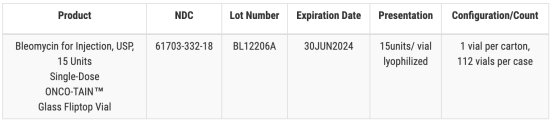
Hospira 在 FDA 網(wǎng)站上發(fā)布的一份通知中表示,就注射抗癌藥博萊霉素而言(一個(gè)批次,,15 個(gè)單位的產(chǎn)品),,一份經(jīng)確認(rèn)的客戶報(bào)告提醒 Hospira 注意單個(gè)小瓶中存在玻璃顆粒。
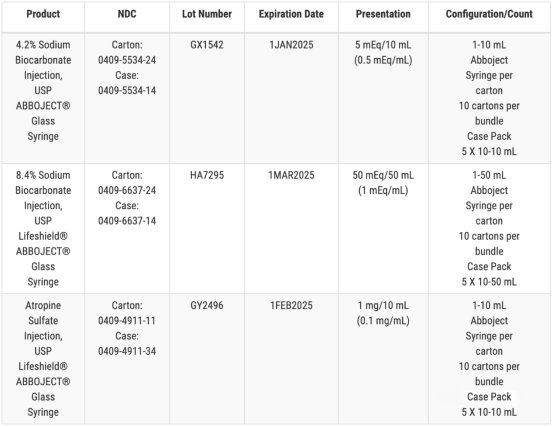
另一召回涉及三種藥物,,包括兩種規(guī)格的注射用碳酸氫鈉,,以及一批硫酸阿托品注射劑。在 Hospira 的例行產(chǎn)品檢查中標(biāo)記為“可能存在玻璃顆粒物質(zhì)”,。輝瑞和 Hospira 均表示,,截至 12 月 21 日,他們尚未收到任何副作用或安全性報(bào)告,。
可見顆粒污染可能會(huì)產(chǎn)生嚴(yán)重的安全后果,,關(guān)乎病人的生命安全。Hospira 警告指出,,如果患者接受了被玻璃污染的藥物,,可能會(huì)發(fā)生“嚴(yán)重不良事件”。潛在的并發(fā)癥可能包括靜脈炎癥和肉芽腫的形成,,或因感染和炎癥,、刺激物或異物反應(yīng)而出現(xiàn)的微小白細(xì)胞和組織簇。Hospira 還警告指出,,注射含有玻璃顆粒的藥物也可能會(huì)阻塞血管并導(dǎo)致危及生命的凝血事件,。
這不是 Hospira 的第一次召回事件,去年 12 月底,,Hospira 召回了一批 1.5g 劑量的抗生素鹽酸萬古霉素,,原因是小瓶中有玻璃顆粒。10 月份,,召回了一批有效期為 2024 年 8 月的 4.2% 的碳酸氫鈉注射劑,,同樣是玻璃顆粒問題。Hospira 還召回了一批有效期為 2024 年 6 月的 1% 鹽酸利多卡因注射劑和一批有效期為 2024 年 7 月的 2% 鹽酸利多卡因注射劑,。
輝瑞于 2015 年以 170 億美元收購的 Hospira 一直召回不斷,。早在2017 年和 2018 年,Hospira 就因一批 25% 嬰兒葡萄糖注射液的注射器中發(fā)現(xiàn)顆粒、微生物生長和人類毛發(fā)問題而多次召回注射液,。
為什么注射液中會(huì)有這么多顆粒呢?因?yàn)樵谧⑸湟旱纳a(chǎn),、儲(chǔ)存、運(yùn)輸,、配置和使用過程中幾乎都有可能被不溶性微粒污染,。做好藥品可見異物/不溶性微粒的風(fēng)險(xiǎn)控制,是確保藥品安全性和有效性的重要措施,。
《中國藥典2020版:0904可見異物檢查法》中規(guī)定:采用燈檢法進(jìn)行結(jié)果判定時(shí),,供試品中不得檢出塊狀物、金屬屑,、玻璃屑,、纖維、絮狀物,、點(diǎn)狀物等明顯的可見異物,。
為此,海岸鴻蒙研制出了對(duì)應(yīng)材質(zhì)的可見異物微粒標(biāo)準(zhǔn)物質(zhì),,可增強(qiáng)生產(chǎn)中的質(zhì)量管理,,溯源可見異物來源,制定可見異物解決方案,,助力企業(yè)的自我挑戰(zhàn),。
海岸鴻蒙作為深耕二十七載的標(biāo)準(zhǔn)物質(zhì)研發(fā)生產(chǎn)企業(yè),顆粒標(biāo)準(zhǔn)物質(zhì)的研發(fā)已經(jīng)達(dá)到國內(nèi)領(lǐng)先,、國際先進(jìn)水平,,可見異物等百余種標(biāo)準(zhǔn)物質(zhì)的研制成功填補(bǔ)國內(nèi)空白,并可提供特殊定制服務(wù),。

最新動(dòng)態(tài)
更多


 手機(jī)版:
手機(jī)版:
虛擬號(hào)將在 秒后失效
使用微信掃碼撥號(hào)