�Ї�(gu��)���w�W(w��ng)Ӎ ����,����(gu��)��ˎ�O(ji��n)�ֺ˲����İl(f��)���ˡ���ˎ�ڷ����w�Ƅ����g�a(ch��n)Ʒ��ŕr(sh��)���о����g(sh��)ָ��(d��o)ԭ�t��,�����£�
��ˎ�ڷ����w�Ƅ����g�a(ch��n)Ʒ��ŕr(sh��)���о����g(sh��)ָ��(d��o)ԭ�t
һ������
��ˎ�ڷ����w�Ƅ������g�a(ch��n)Ʒ�|(zh��)���������a(ch��n)�^(gu��)�̿��Ƶ��P(gu��n)�I����,����ˎƷ�����|(zh��)����(bi��o)��(zh��n)����Ҫ���C��ԓ��Ƅ���ˇͨ����������(g��)���a(ch��n)����,�������a(ch��n)���ŵ�ԭ���܌�(d��o)�����g�a(ch��n)Ʒ�o(w��)�����r(sh��)�M(j��n)����һ�������a(ch��n)����Ҫ�������r,��ˎƷע��(c��)��Ո(q��ng)��/���a(ch��n)��I(y��)���аl(f��)�����a(ch��n)�^(gu��)���Б�(y��ng)�P(gu��n)ע���g�a(ch��n)Ʒ�Ĵ�ŕr(sh��)���о�,����ŕr(sh��)����ָ���g�a(ch��n)Ʒ���ض��l���´�Ų��ܾS������ϼȶ����|(zh��)����(bi��o)��(zh��n)�ĕr(sh��)�g�L(zh��ng)�ȡ����M(j��n)һ���ӏ�(qi��ng)��(gu��)�H����ˎƷע��(c��)���g(sh��)�f(xi��)�{(di��o)��(hu��)�|(zh��)��Դ���O(sh��)Ӌ(j��)�����ڌ�(sh��)�H���a(ch��n)�е��\(y��n)��,�����ˎ�ڷ����w�Ƅ����a(ch��n)�^(gu��)���е��L(f��ng)�U(xi��n)����ˮƽ�����_���g�a(ch��n)Ʒ��ŵ����P(gu��n)���g(sh��)Ҫ��,���ƶ���ָ��(d��o)ԭ�t��
��ָ��(d��o)ԭ�t�m���ڻ�ˎ�ڷ����w�Ƅ�,��ּ�ڽ�Q�Ƅ����I(y��)���P(gu��n)ע�Ļ�ˎ�ڷ����w�Ƅ��ڷ��B�m(x��)���a(ch��n)�r(sh��)��ͬ���a(ch��n)���������g�a(ch��n)Ʒ��Ҫ�̕����A�Ć�(w��n)�},�����ڞ�ˎ���аl(f��)�����a(ch��n)�^(gu��)�������g�a(ch��n)Ʒ�Ĵ�ŕr(sh��)���о��ṩ���g(sh��)ָ��(d��o)�ͅ���,��ͨ����r����(d��ng)�Ƅ�����(g��)���a(ch��n)�^(gu��)�̳��^(gu��)30��r(sh��),����(y��ng)�M(j��n)�����g�a(ch��n)Ʒ��ŕr(sh��)���о�����(d��ng)�Ƅ�����(g��)���a(ch��n)�^(gu��)�̲����^(gu��)30��r(sh��),����(y��ng)ͨ�^(gu��)�L(f��ng)�U(xi��n)�u(p��ng)���Q���Ƿ���Ҫ�M(j��n)�����g�a(ch��n)Ʒ��ŕr(sh��)���о�,��
ˎƷע��(c��)��Ո(q��ng)��/���a(ch��n)��I(y��)����؟(z��)�����w,����(y��ng)�Y(ji��)�Ϯa(ch��n)Ʒ�����a(ch��n)��ˇ�����c(di��n),����(du��)����Ӱ����g�a(ch��n)Ʒ�|(zh��)������������b��ʽ����ŭh(hu��n)�����ض�,����ȵȣ����M(j��n)���L(f��ng)�U(xi��n)�u(p��ng)��,���O(sh��)Ӌ(j��)������ȡ��Ӌ(j��)�����x��Ӱ��Ƅ����a(ch��n)�����P(gu��n)�I�|(zh��)�����Ե��(xi��ng)Ŀ���鿼��ָ��(bi��o),���ṩ֧�����о�����(j��)���C����ŕr(sh��)�ĺ����ԡ�
��ָ��(d��o)ԭ�t�H����ˎƷ�O(ji��n)�ܲ��T��(d��ng)ǰ���^�c(di��n)���J(r��n)�R(sh��),���S���ƌW(xu��)�о����M(j��n)չ,����ָ��(d��o)ԭ�t�е����P(gu��n)��(n��i)�����������c����,����(y��ng)�ñ�ָ��(d��o)ԭ�t�O(sh��)Ӌ(j��)�͌�(sh��)ʩ�о��r(sh��),����ͬ�r(sh��)����ˎƷ���a(ch��n)�|(zh��)������Ҏ(gu��)����������(gu��)��(n��i)�����P(gu��n)�ļ��g(sh��)�ļ�,��
������Ҫ�о�?j��)?n��i)��
��һ����ƷҪ��
���g�a(ch��n)Ʒ�Ĵ�ŕr(sh��)���о���(y��ng)��������ԇҎ(gu��)ģ�������M(j��n)��,������о�����δ�_(d��)���̘I(y��)��Ҏ(gu��)ģ���t����Z���̘I(y��)��Ҏ(gu��)ģ�����w�M�������a(ch��n)��(ch��ng)�أ����M(j��n)�д_�J(r��n),����(d��ng)�a(ch��n)Ʒ̎�������a(ch��n)��ˇ,���O(sh��)�䡢�A�ؗl���Ͱ��ĵȰl(f��)��׃���r(sh��),����ͨ�^(gu��)�L(f��ng)�U(xi��n)�u(p��ng)����(l��i)�ж��Ƿ���Ҫ��(du��)��ŕr(sh��)���M(j��n)�������о����ٴδ_�J(r��n)��
�����x��һ�����g�a(ch��n)Ʒ��(l��i)�_����ŕr(sh��)��,��Ҳ�ɻ������ϵ����Ժ��������P(gu��n)����,��ͨ�^(gu��)�L(f��ng)�U(xi��n)�u(p��ng)����(l��i)�_���m��(d��ng)?sh��)����Ρ?/p>
��(du��)�ڶ�Ҏ(gu��)���Ƅ������Ի����L(f��ng)�U(xi��n)�u(p��ng)���x������Ե�Ҏ(gu��)���(l��i)�M(j��n)���о�,��
�������о���(du��)����r(sh��)�g�Ϳ����(xi��ng)Ŀ
��ͬ�a(ch��n)Ʒ��(y��ng)�Y(ji��)�τ���,�����a(ch��n)��ˇ�����c(di��n),����(du��)���a(ch��n)�^(gu��)���M(j��n)�з���������(j��)��Ҫ������A�����a(ch��n)�^(gu��)�̵ĕr(sh��)�g,���Լ��h(hu��n)���ʹ��A�l���ĝ���Ӱ푴_���������о���(du��)��
�_���о���(du��)���,����(y��ng)�Y(ji��)�ϲ�ͬ���a(ch��n)���������g�a(ch��n)Ʒ�����Ժʹ��A����,�����Y(ji��)���о���(du��)��(du��)���m(x��)��ˇ���Ƅ��P(gu��n)�I�|(zh��)�����Ե�Ӱ푣��O(sh��)����ͬ�Ŀ���r(sh��)�g�c(di��n),���r(sh��)�L(zh��ng)�Ϳ����(xi��ng)Ŀ,�,�������(xi��ng)Ŀ��(y��ng)�ܷ�ӳ���g�a(ch��n)Ʒ�|(zh��)����׃����r�����ڷ����^(gu��)�����װl(f��)��׃����,������Ӱ푳�Ʒ�|(zh��)��,����ȫ�Ժ�/����Ч�Ե��(xi��ng)Ŀ,����(n��i)��ͨ�����w���������W(xu��)������W(xu��)������,����ŕr(sh��)���о��ij��m(x��)�r(sh��)�g��(y��ng)ԓ���w�M�������L(zh��ng)��ŕr(sh��)�g������r(sh��)�g�c(di��n)��(y��ng)���ٰ����_(k��i)ʼ�����g�ͽY(ji��)���r(sh��)�g,��
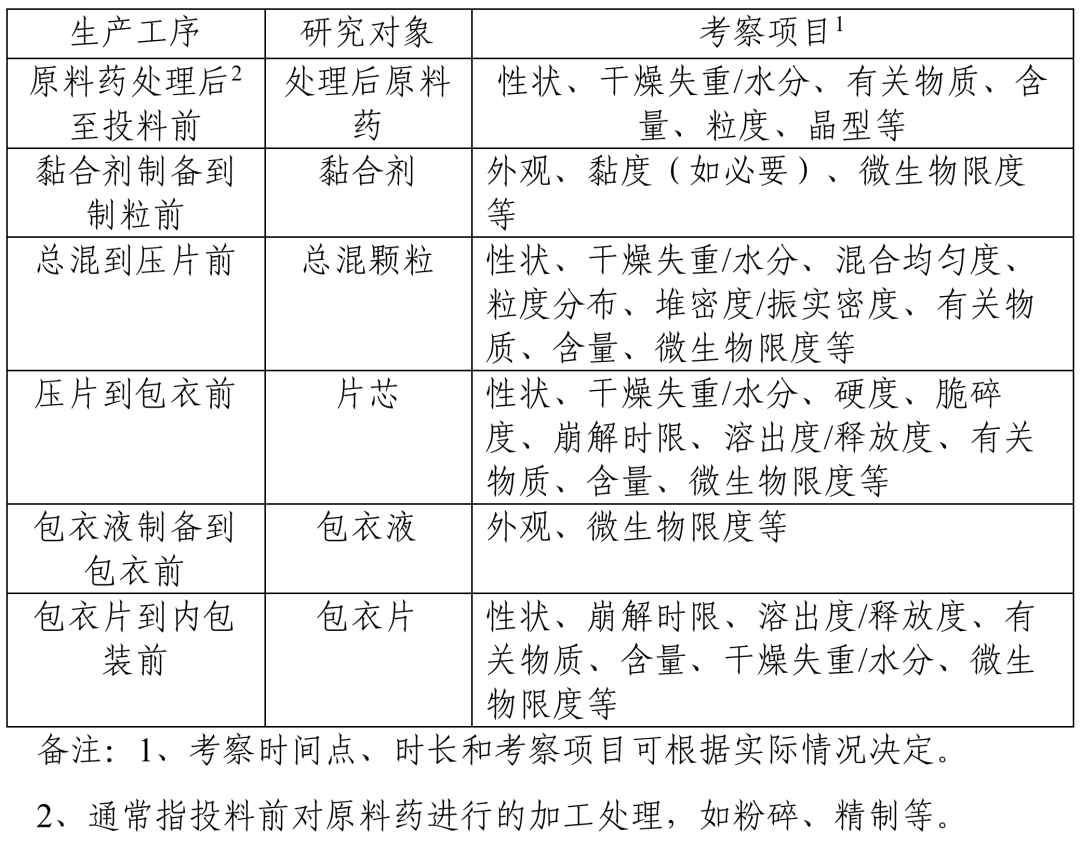
�Կڷ�����Ƭ������,���±����e�����P(gu��n)��ŕr(sh��)�����a(ch��n)�����о���(du��)��,�������(xi��ng)Ŀ��Ҋ(ji��n)ʾ��������ָ��(d��o)ԭ�t���]�����a(ch��n)����,���о���(du��)�����(xi��ng)Ŀ�Ȳ��������������a(ch��n)��r��ˎƷע��(c��)��Ո(q��ng)��/���a(ch��n)��I(y��)�ɸ���(j��)�������c(di��n)�����a(ch��n)��Ҫ���Y(ji��)�Ϯa(ch��n)Ʒ��(w��n)������r,������(j��)��ָ��(d��o)ԭ�t�о�˼·�������L(f��ng)�U(xi��n)�u(p��ng)���M(j��n)���x����{(di��o)��,��
ʾ�� �ڷ�����Ƭ����ŕr(sh��)�����a(ch��n)����,���о���(du��)�����(xi��ng)Ŀ
�������о���Ʒ�Ĵ�ŗl��
��ŗl������(y��ng)��(du��)���m(x��)�����a(ch��n)��ˇ�Լ����g�a(ch��n)Ʒ�ķ�(w��n)���ԡ��|(zh��)��,����ȫ�Ժ�/����Ч�Ԯa(ch��n)������Ӱ푡���(sh��)�H�о��н��h�ƶ���ŕr(sh��)���о�����,���о���Ʒ�Ĵ�ŗl����(y��ng)���]����(n��i)�ݣ���1����Ʒ��ŵĭh(hu��n)���l����(y��ng)�c����^(q��)��ėl���ஔ(d��ng)����t��(y��ng)�f(shu��)�������l���ĺ�����,����2����Ʒ�ĕ���������(y��ng)�c�̘I(y��)�����a(ch��n)��Ʒ�������õ�������ͬ,������ڴ�ŕr(sh��)�����б�횜pС�����ߴ磬��(y��ng)ʹ�õ�ͬ�����������|(zh��)��ͬ,��ʹ���c���a(ch��n)��ͬ�����]ϵ�y(t��ng)�������M(j��n)�к�����Փ�C����3����(du��)���з�(w��n)�����L(f��ng)�U(xi��n)�������������Įa(ch��n)Ʒ,�������^(gu��)���Б�(y��ng)�P(gu��n)ע���g�a(ch��n)Ʒ������픲����g��(du��)�a(ch��n)Ʒ�|(zh��)���ĝ���Ӱ�,����Ҫ�r(sh��)��ŕr(sh��)���о���(y��ng)���]������Εr(sh��)�ėl����픲����g�c������������ı�����(y��ng)���ٺͳ�Ҏ(gu��)���a(ch��n)�п��ܵ����������ͬ���eҪ���]δ�b�M������,��
������ڿ��(ch��ng)���D(zhu��n)�ƣ�߀��(y��ng)���]�D(zhu��n)�ƕr(sh��)�g���D(zhu��n)�Ɨl��,����Ҫ�r(sh��)�M(j��n)�м���ԇ�(y��n)���C������ƫ�x���A�l���r(sh��)�ķ�(w��n)���ԡ�
���ģ��|(zh��)����(bi��o)��(zh��n)�c��������
����(j��)�a(ch��n)Ʒ���c(di��n)���|(zh��)��������Ҫ�����O(sh��)�����g�a(ch��n)Ʒ��ŕr(sh��)���о����|(zh��)����(bi��o)��(zh��n),�������õķ���������(y��ng)��(j��ng)�^(gu��)�����W(xu��)�(y��n)�C���ܝM���о���Ҫ��
���壩��ŕr(sh��)�Ĵ_��
��(y��ng)����(j��)���g�a(ch��n)Ʒ�ķ�(w��n)�����о��Y(ji��)���͌�(sh��)�H���a(ch��n)��Ҫ�M�������Ĵ�ŕr(sh��)��,����Ҫ�r(sh��)����(y��ng)�����@�õĔ�(sh��)��(j��)�M(j��n)�нy(t��ng)Ӌ(j��)�W(xu��)�о�,������׃��څ��(sh��)�����ж��������(xi��ng)Ŀ�M�����c��ŕr(sh��)���O(sh��)���ĺ�����,��������g�a(ch��n)Ʒ�ڴ�ŕr(sh��)���о����g��(n��i)���о���(sh��)��(j��)�@ʾ�к������͡�����a(ch��n)�����ӵ�����,���t��(y��ng)���]��(du��)��(j��ng)���L(zh��ng)��ŕr(sh��)���о������g�a(ch��n)Ʒ�Ƶõij�Ʒ�����M(j��n)�м���/�L(zh��ng)�ڷ�(w��n)����ԇ�(y��n)���߿��]�s�����g�a(ch��n)Ʒ�Ĵ�ŕr(sh��)���Դ_�����a(ch��n)���ϸ���Ƅ���Ʒ,��
������(l��i)Դ��
��(gu��)��ˎƷ�O(ji��n)��������ˎƷ���u(p��ng)����
���Ї�(gu��)���w�W(w��ng)������/���裩
ע���DƬ���̘I(y��)��;,�������֙�(qu��n)��֪?ji��ng)h��